

“医疗物资出口产地检验”事件一波三折。海关最新消息指出,按照72号文件要求,对于53号公告规定的11类(19个商品编码)出口法检医疗物资,采取的是验证管理方式,意味着无需实施产地检验,报关时不需要出口电子底账,企业正常申报报关单。
有业内人士指出,虽然目前实际操作中,仍是按照之前的正常申报,且不会被退单,但几乎99%都会被查验,出口通关审核趋严。
口罩等防疫物资资质梳理,美国和欧洲当地资质要求各异
据卖家爆料称:“自上周开始,欧洲ECM认证机构已经停止接单,就连FDA也全面停止接单了。身边已有同行口罩机都已准备就绪,非要安装好后再进行申请认证,奈何机器安装到一半认证通道却关闭了,巧妇难为无米之炊。”
对此,深圳合众商务咨询有限公司副总经理张剑表示,尽管当前海关公告明确指出医疗物资出口无需实施产地检验,但出口企业切忌掉以轻心,不排除未来医用口罩等防疫物资会被列为出口法检的可能。因此,建议出口企业应积极准备法检合规产品,对接合规且有资质的厂家,如果是手头仍有库存的情况下,则尽快将产品发往海外才是明智之举。
据介绍,从事口罩等防疫物资的出口企业,应在口岸报关前向生产地、组货地海关提出申请,且满足产品生产和发货地资质要求,以及产品销售地资质要求。
1、产品的生产和发货地资质要求:主要包括海关出口、行业政府监管,以及工厂出厂生产这三点。
以口罩出口为例,包括如下几点:
(1)生产厂家需要提供有第三方检测机构提供的口罩产品检测报告;
(2)行业监管要求,需要销售口罩的公司具备医疗器械产品销售资质,口罩等一般防疫物资需要申请国内二类医疗备案许可资质;
(3)海关要求,销售口罩的公司要具备货物出口权资质。
2、产品的销售地资质要求
其一、美国当地。
目前,美国当地的行业监管及海关监管,需要对防疫物资具备FDA资质认证才可以进口清关。
那么,美国FDA认证需要具备哪些条件呢?目前,美国对口罩认证分为两种,一种是需要注册一类FDA认证的防护口罩;另一种是需要二类FDA认证的医用口罩。
张剑表示,通常情况下二类FDA认证时间长达十个月,且注册费用昂贵接近20万人民币,国内真正意义上申请二类FDA认证的医用口罩出口企业屈指可数。另有官网数据显示,最近三年中国企业获得美国FDA二类认证的企业是个位数。
“目前大多数企业的做法是把防护口罩和符合医用标准的医用口罩都只能按照防护类口罩申请一类FDA认证,这就导致KN95口罩(属于医用口罩)在清关时被抽查容易触发潜在风险。口罩是医用标准还是防护标准,只能在国内采购时与厂家或是供应商确定好产品规格,目前大家的做法就是把防护口罩和医用口罩都在FDA一类防护口罩申请认证资质,现在国内几乎是找不到具备FDA二类认证的工厂厂家。”他透露。
其二、欧洲当地。
欧洲口罩等防疫产品需要具备CE认证,CE认证对口罩也分为防护口罩和医用口罩两种。就目前来看,国内的商家通常申请的大多数是CE防护口罩认证资质,防护等级FFP2,执行标准EN149-2009。
据张剑介绍,中国卖家申请CE认证,需要具备在欧洲当地的认证机构递交认证申请,可以自由选择认证机构。而如果在国内申请CE认证,只能通过当地机构授权给国内认证机构的机构才可以申请成功。“目前尚无可定论哪家机构的证书是真实有效,每一份CE证书会对应一份产品检测报告,没有检测报告的CE证书将面临巨大的商业风险和法律风险。”
除此之外,针对CE在欧洲清关货物被扣的问题。一位不具名的资深物流服务人士坦言,当前跨境服务市场鱼龙混杂,不排除会有部分不专业且不负责任的企业会把防护口罩申报和医用口罩申报混为一谈,打着口罩检测报告名义进行清关,最终导致被海关查验扣货。他强调,“尤其是从事口罩等防疫物资的出口企业,凡是提供有效的CE认证,不要轻易在清关时申报高规格口罩标准,确保口罩产品品质有保障,才能大大降低产品被扣货的几率。”
海关53号文件“余震”,外贸B2B和跨境B2C如何对症下药?
“外贸B2B和跨境B2C对于医用口罩等防疫物资出口具备资质实际上大有不同,这往往也是出口企业容易忽视之处。”张剑分析道,一种是外贸B2B的企业通常都会有自己的进出口权公司,具备货物进出口资质,公司的货物出口是采用自己的进出口权公司进行出口报关及出口退税;另一种跨境B2C卖家,大部分是不做出口退税,货物出口清关主要是外包交由专业FBA头程公司一站式解决,支付相应运费即可。仅有少数卖家会做小部分出口退税,这类卖家中还有一部分是用物流公司的资质做出口退税的情况,实则拥有进出口资质的公司少之又少。
随着海关53号文件出台,不同类型出口企业面临的难题各异。“一方面,对于已经拥有货物进出口资质的外贸B2B企业,只需要在原来的基础上,增加海关产品检验检疫资质备案申请,申请国内二类医疗备案销售许可资质。上游供应商提供第三方权威机构出具的产品检测报告,只要产品品质符合相关要求即可符合海关最新的出口条件了;另一方面,大多数跨境B2C卖家不具备货物进出口权的资质,有的卖家用自己不具备货物进出口权的公司申请了国内二类医疗备案许可。”他说。
卓志跨境电商总裁李金玲也针对医疗物资出口,通关单填报的注意事项提出如下几点:
1、领证机关:企业申请电子底账的属地海关代码;
2、品名,商品编码,品牌,型号,成交单位,成交数量,货物总值保持与报关资料一致;
3、通关单信息中的境内发货人、运抵国、项数、次序与报关信息确保一致;
4、出口货物报关单上的“申报日期”必须在出境货物通关单的有效期内。需要注意的是,目前申报系统已升级,通关单数量和项数要与报关单一致,否则将无法通过审核。
根据商务部、海关总署、国家药品监督管理局发布的2020年第5号最新公告指出,自4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的企业向海关报关时,须提供书面或电子声明(模版如下图所示),承诺出口产品已取得中国医疗器械产品注册证书,从而符合进口国(地区)的质量标准要求。海关将凭药品监督管理部门批准的医疗器械产品注册证书验放。
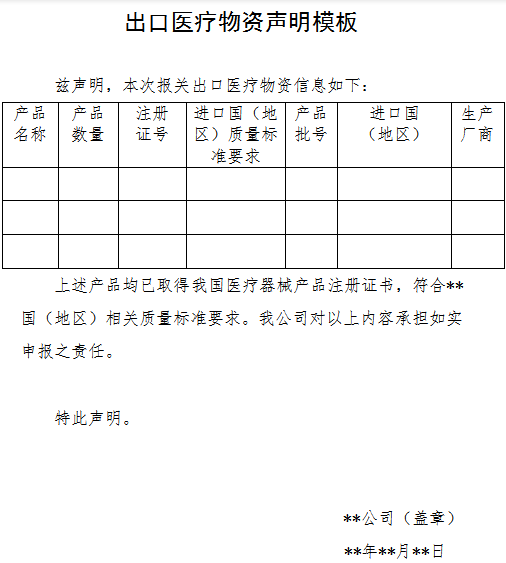
(出口医疗物资声明模版截图)
最后,张剑总结道:“不论口罩是否需要检验,这对于从事口罩等防疫物资的企业来说,当务之急是尽快有一家自己的公司,具备货物进出口权资质,获得海关检验检疫备案许可,申请国内二类医疗器械销售许可。与此同时,出口产品品质应当符合相关行业标准,产品具备国内第三方权威检测机构出具的产品检测报告,未雨绸缪做好万全准备,以不变应万变。”
(文/雨果网 陈林)
【特别声明】未经许可同意,任何个人或组织不得复制、转载、或以其他方式使用本网站内容。转载请联系:editor@cifnews.com
相关阅读推荐: